Naukowcy z Zakładu Genetyki oraz Zakładu Patologii i Diagnostyki Laboratoryjnej NIO-PIB we współpracy z Międzynarodowym Instytutem Biologii Molekularnej i Komórkowej w Warszawie, liderem projektu finansowanego z Narodowego Centrum Nauki, odkryli nowy cel dla terapii przeciwnowotworowej.
W najnowszej pracy opublikowanej w prestiżowym czasopiśmie „EMBO Molecular Medicine” zespół kierowany przez prof. Martę Miączyńską z Międzynarodowego Instytutu Biologii Molekularnej i Komórkowej przy udziale pracowników oraz zaplecza badawczego NIO-PIB, w tym pracowni heteroprzeszczepów, zidentyfikował gen VPS4A jako cel molekularny dla spersonalizowanej terapii przeciwnowotworowej opartej na syntetycznej letalności.
Rearanżacje genomu (na przykład amplifikacje lub utraty fragmentów chromosomów) obejmujące geny kluczowe dla komórki stanowią siłę napędową transformacji komórki prawidłowej w nowotworową. Paradoksalnie te same zmiany genetyczne mogą także doprowadzić do powstania tak zwanej „pięty achillesowej”. Dzieje się tak na przykład w sytuacji, gdy wraz z usuniętym fragmentem genomu tracony jest gen X, który w prawidłowej komórce współpracuje z innym genem Y w przebiegu ważnych dla życia komórki procesów. Wówczas pozostały gen Y staje się „piętą achillesową” komórki nowotworowej, ponieważ jego farmakologiczne wyłączenie spowoduje śmierć komórki nowotworowej. Zjawisko to definiowane jako syntetyczna letalność (ang. synthetic lethality) i stanowi obiecujące podejście dla rozwijania nowych celowanych terapii w onkologii.
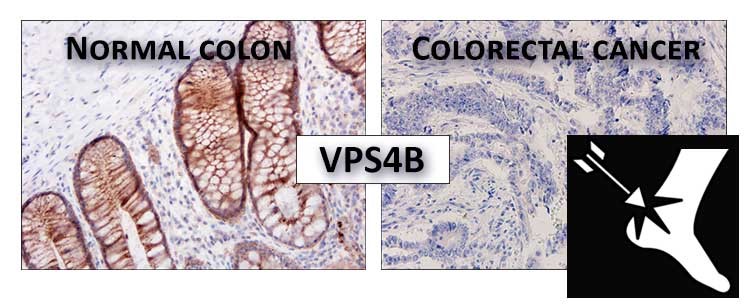
W wielu nowotworach, a szczególnie w raku jelita grubego, gen VPS4B, kodujący enzym o aktywności ATPazy, ulega częstej utracie wraz z fragmentem chromosomu 18, co powoduje, że komórki nowotworowe mogą być szczególnie wrażliwe na zahamowanie aktywności siostrzanego białka VPS4A.
Wykorzystując ludzkie linie nowotworowe hodowane w warunkach in vitro i in vivo, naukowcy udowodnili, że geny VPS4A i VPS4B wykazują syntetyczną letalność, tj. obniżenie poziomu obu kodowanych przez nie białek jednocześnie (VPS4A+B) powodowało śmierć komórek, podczas gdy obniżenie poziomu każdego z nich pojedynczo było tolerowane przez komórkę. Wyniki te wskazują, że komórki nowotworowe z obniżonym poziomem białka VPS4B są wyjątkowo wrażliwe na zaburzenia aktywności białka VPS4A („pięta achillesowa”). Dodatkowo autorzy pracy odkryli, że komórki umierające z powodu braku obu białek VPS4 indukują silną odpowiedź zapalną, która w warunkach organizmu może wywoływać reakcję przeciwnowotworową, co potencjalnie może mieć dodatkowy, korzystny wpływ na wynik terapii.
Podsumowując: odkrycia zespołu stanowią ważny fundament dla przyszłych badań mających na celu opracowanie farmakologicznych inhibitorów ATPaz VPS4, jako potencjalnych leków w celowanej terapii nowotworów z obniżonym poziomem VPS4B, w tym nowotworów jelita grubego.
Źródło:
Synthetic lethality between VPS4A and VPS4B triggers an inflammatory response in colorectal cancer
Ewelina Szymańska, Paulina Nowak, Krzysztof Kolmus, Magdalena Cybulska, Krzysztof Goryca, Edyta Derezińska-Wołek, Anna Szumera-Ciećkiewicz, Marta Brewińska-Olchowik, Aleksandra Grochowska, Katarzyna Piwocka, Monika Prochorec-Sobieszek, Michał Mikula, Marta Miączyńska






